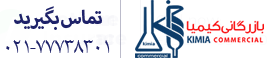حل شدن شکر در آب

امولسیفایر
24/10/1399
سیستم بویایی انسان
03/11/1399انحلال شکر در آب را تغییر فیزیکی بدانیم یا تغییر شیمیایی؟
یکی از کارهایی که روزانه و به دلایل مختلف انجام می دهیم، حل کردن شکر در آب است. شاید بتوانیم بگوییم همه ما از همان کودکی باید در کنار سفره صبحانه یک لیوان چای شیرین داشته باشیم و این عادت صبحانه چای شیرین برای خیلی از افراد ترک نشدنی است.
شما که در حال خواندن این مطلب هستید، به شیمی علاقه دارید و یا به دنبال کسب اطلاعات بیشتر در زمینه شیمی هستید و از این طریق قصد دارید پاسخ برخی از سوالات ساده در زمینه شیمی را بیابید. پس با نگاهی شیمیایی می خواهیم بررسی کنیم آیا حل شدن شکر در آب تغییری شیمیایی به شمار می رود یا تغییر فیزیکی؟
چه تغییراتی فیزیکی و چه تغییراتی را شیمیایی می نامند؟
گاهی برای پاسخ دادن به سوالات شیمی ساده نیاز است با برخی اصول و مفاهیم پایه ی شیمی آشنا باشیم. ازجمله مفاهیم ساده در شیمی تعریف واکنش شیمیایی و اطلاع از تغییرات فیزیکی و شیمیایی حاصل از آن است.
خوب است در اینجا تعریفی مختصر از واکنش شیمیایی را با هم مرور نماییم و در ادامه نحوه تشخیص تغییرات فیزیکی یا شیمیایی را بررسی نماییم.

واکنش شیمیایی : فرآیندی که طی آن ساختار ذرات تشکیل دهنده مواد اولیه به دلیل تأثیر بر یکدیگر تغییر کرده و مواد شیمیایی جدیدی به عنوان محصول تبدیل می شود.
تغییراتی که در طی یک واکنش بین واکنش دهنده ها صورت می گیرد را می توان به دو دسته تغییر فیزیکی و تغییر شیمیایی تقسیم نمود.
در تغییر فیزیکی تنها حالت ماده تغییر کرده و در ساختار ذرات تشکیل دهنده آن هیچ تغییری ایجاد نمی شود. به همین دلیل تغییر حالت های ماده ازجمله تبخیر، تصعید، میعان، ذوب، انجماد و چگالش را در دسته تغییرات فیزیکی قرار می دهند.
برعکس در تغییر شیمیایی، تغییر در آرایش الکترونی اتم ها و نحوه اتصال آنها به یکدیگر را شاهد هستیم. به همین دلیل می توان گفت مواد جدید که ویژگی های متفاوتی دارند در اثر یک تغییر شیمیایی حاصل می شود.
به هنگام حل شدن شکر در آب چه رخ می دهد؟

زمانی که یک قاشق شکر را در یک لیوان آب حل می کنید، در ابتدا بخش عمده ای از آن شکر در آب به طور خودبه خود حل می شود ولی برای انحلال کامل شکر در آب اغلب از یک قاشق برای هم زدن استفاده می کنید. پس از چند لحظه شکر به طور کامل در آب حل شده و هیچ نشانه ای از آن را مشاهده نمی کنید؛ ولی اگر کمی از این آب را بنوشید، طعم شکر را تشخیص می دهید. به عبارت دیگر، علت شیرین شدن آب پراکنده شدن مولکول های شکر به طور کامل در آب است.
نکته : برای حل شدن دو ماده در هم باید یک محلول و یک حلال داشته باشیم. حلال ماده ای است که ماده حل شونده را از طریق تجزیه در خود حل می کند.
در نمونه شکر و آب، شکر نقش حل شونده و آب نقش حلال را دارد.
با توجه به اینکه آب و شکر هر دو مولکول های قطبی دارند، مولکول های آب از طرف قطب مخالف به مولکول های شکر نزدیک شده و به دلیل بیشتر بودن نیروی جاذبه بین قطب های مختلف نسبت به نیروی بین مولکولی در شکر، مولکول های شکر از یکدیگر جدا شده و در آب حل می شوند.
با توجه به اینکه در اثر انحلال شکر در آب، ویژگی های مولکول های شکر تغییری نمی کند، می توان گفت حل شدن شکر در آب یک تغییر فیزیکی است.
اما این شرایط برای ترکیب یونی مانند نمک متفاوت است. اگر ترکیبات یونی مانند نمک در آب حل شوند، با توجه به اینکه خواص نمک با یون های حاصل از انحلال نمک در آب متفاوت است، می توان نتیجه گرفت تغییر حاصل یک تغییر شیمیایی است. علاوه براین، از طریق تبخیر آب، نمک حل شده در آب باقی می ماند و شاید این باعث شود که برخی به اشتباه تصور کنند حل شدن نمک در آب یک تغییر فیزیکی است.
میزان انحلال پذیری در یک محلول
لازم است بدانید ساختار شیمیایی حلال و حل شونده میزان انحلال پذیری مواد را تعیین می کند. زیرا براساس ساختار شیمیایی، نوع نیروهای جاذبه موجود در محلول مشخص می شود. بنابراین رابطه بین حلال و حل شونده میزان انحلال پذیری در محلول را تعیین می کند؛ به گونه ای که می توان گفت هرچه برهمکنش میان حلال و حل شونده بیشتر باشد، میزان انحلال پذیری نیز بیشتر خواهد بود.
این گونه می توان بیان کرد که حل شونده های قطبی در حلال های قطبی و حل شونده های غیرقطبی در حلال های غیرقطبی به خوبی حل می شوند.

البته میزان حل شدن هر ماده ای در حلال خود با محدودیت هایی روبه رو است. زیرا حل شونده تا حدی می تواند در حلال حل شود که در اصطلاح به آن نقطه اشباع می گویند. نقطه اشباع نقطه ای است که دیگر محلول قادر به حل کردن مقدار بیشتر حل شونده نخواهد بود.
به کمک هم زدن، تغییر دمای محلول و یا تغییر فشار می توان قدرت محلول در حل کردن را افزایش داد.
تاثیر دما بر انحلال پذیری
تغییر دما در یک محلول، بر میزان انحلال پذیری جامد، مایع و گاز تأثیرات متفاوتی دارد.
برای یک جامد، تأثیر دما بر میزان حل شدن آن به گرماده یا گرماگیر بودن واکنش حاصل از انحلال بستگی دارد. فرض کنید واکنش مد نظر گرماگیر است. یعنی واکنش تمایل دارد با دریافت گرما از محیط به سمت تبدیل واکنش دهنده ها به فرآورده ها حرکت نماید. بنابراین می توان گفت در واکنش های گرماگیر، با افزایش دما میزان انحلال پذیری جامدات افزایش می یابد.
درحالیکه این امر برای واکنش های گرماده برعکس است. به عبارت دیگر، در واکنش های گرماده با آزاد کردن انرژی، واکنش دهنده ها به فرآورده ها تبدیل می شوند. بنابراین اگر به چنین واکنش هایی گرما دهیم، در جهت عکس یعنی تبدیل فرآورده ها به واکنش دهنده ها حرکت می کند؛ درنتیجه میزان انحلال پذیری جامدات در واکنش های گرماده با افزایش دما کاهش می یابد.
برای بررسی تأثیر دما بر انحلال پذیری گازها می بایست با تعریف انرزی جنبشی آشنا باشید. همان طور که می دانید با افزایش دما، انرژی جنبشی نیز افزایش می یابد. افزایش انرژی جنبشی نیز باعث افزایش حرکت ذرات مولکولی می شود. بنابراین می توان گفت با افزایش دما، انحلال پذیری گازها کاهش می یابد. زیرا با افزایش انرژی جنبشی، ذرات گاز محلول تمایل به ازاد شدن داشته و ذرات گاز نامحلول کمتری نیز تمایل به حل شدن دارند.
در گازها کاهش دما انحلال پذیری انها را افزایش می دهد.
اما برای مایع ها نمی توان مانند جامدات و گازها یک اصل کلی را بیان نمود.
تأثیر فشار بر انحلال پذیری
این تدثیر را تنها می توان برای گازها بررسی نمود. زیرا در مایعات و جامدات افزایش فشار تأثیر قابل ملاحظه ای را اعمال نمی کند. اما تأثیر افزایش فشار بر میزان انحلال پذیری گازها را با توجه به اصل هنری و لوشاتلیه می توان توضیح داد.
اینگونه می توان بیان کرد که افزایش فشار باعث افزایش فشار جزئی شده و ذرات بیشتری از گاز را وارد مایع می کند. طبق اصل لوشاتلیه این افزایش حل شوندگی در مقابله با افزایش فشار جزئی است.
قیمت و خرید انواع مواد شیمیایی صنعتی و خوراکی
در صنعت امروز مواد شیمیایی صنعتی و خوراکی کاربردهای بسیاری دارند. بازرگانی کیمیا شیمی پایدار یکی از معتبرترین تأمین کنندگان مواد شیمیایی است که با توجه به اهمیت آنها در صنعت همواره کیفیت محصولات عرضه شده را در اولویت کار خود قرار داده است. شما می توانید جهت خرید انواع مواد شیمیایی به صورت عمده و اطلاع از قیمت آنها و یا دریافت آنالیز مصرف محصولات با کارشناسان فروش تماس حاصل نمایید.
021-77738301
021-77738302
021-77738303